Transition und frühe Diagnose: Herausforderungen bei inflammatorischen Autoimmunerkrankungen
In einer Talkrunde beim 47. Kongress der Deutschen Gesellschaft für Rheumatologie (DGRh) in Dresden griffen ausgewiesene Experten aktuelle Herausforderungen in der Behandlung von inflammatorischen Autoimmunerkrankungen auf. Dazu thematisierten sie unter anderem, wie die Transition in die rheumatologische Versorgung von Erwachsenen und wie eine möglichst frühe Diagnose einer rheumatoiden Arthritis (RA) gelingen kann.
Transition ins Erwachsenenalter
Dr. med. Ivan Földvari, Facharzt für Rheumatologie und Kinder- und Jugendmedizin aus Hamburg erläuterte zunächst, weshalb eine gelungene Transition so bedeutsam ist: So haben etwa 50 Prozent der Patienten mit juveniler idiopathischer Arthritis eine aktive Erkrankung beim Übergang ins Erwachsenenalter. Dabei bleiben auch mögliche Besonderheiten der Erkrankung unabhängig vom Alter bestehen, wie beispielsweise eine Uveitis oder Kiefergelenksbeteiligung, die auch weiterhin adressiert werden müssen, gab der Experte zu bedenken. Das Ziel der Transition ist es, die chronisch kranken Jugendlichen im Umgang mit der Erkrankung, der Medikation und den Nebenwirkungen so zu schulen, dass sie selbständig damit umgehen können.
Viel Kommunikation vonnöten
Auf diesem Weg gilt es jedoch, einige Barrieren zu überwinden, wie beispielsweise eine schlechte Adhärenz beziehungsweise mangelhaftes Wissen über die Behandlung und Medikation seitens des Patienten. Außerdem sind zu wenig kinderrheumatologisch vorgebildete Erwachsenenrheumatologen in der Praxis tätig, so Dr. med. Földvari. Darüber hinaus findet häufig gar keine Kommunikation zwischen Kinder- und Erwachsenenrheumatologen statt.
Jugendliche im Alter von 13 bis 20 Jahren erhoffen sich im Rahmen der Transition vor allem eine Unterstützung bei der beruflichen Orientierung, gefolgt von mehr Informationen über die Behandlung und die Erkrankung. Daher empfiehlt der Experte für die Praxis mindestens zwei gemeinsame Visiten mit Patient, Kinder- und Jugendrheumatologe und Rheumatologe. Auf den gemeinsamen Visiten wird unter anderem eine Anamnese erhoben, das weitere Vorgehen diskutiert, Unklarheiten ausgeräumt sowie Besonderheiten des Patienten berücksichtigt.
Frühe Diagnose RA ermöglichen
PD Dr. med. Rebecca Fische-Betz, Fachärztin für Innere Medizin an der Universitätsklinik in Düsseldorf, hob die Bedeutung einer frühen Diagnose hervor, da eine frühzeitige Behandlung der RA den gesamten weiteren Krankheitsverlauf positiv beeinflussen kann. In Deutschland sollen laut S3-Leitlinie nach Möglichkeit alle an einer RA neu Erkrankten innerhalb von sechs Wochen eine fachspezifische Versorgung erhalten, erläuterte die Expertin. Eine wesentliche Herausforderung stellen die langen Wartezeiten auf einen ersten Termin beim Facharzt dar.
Allein im Versorgungsgebiet Düssel- dorf belaufen sich die Wartezeiten von Neupatienten derzeit häufig auf etwa sechs Monate, so PD Dr. med. Fische-Betz. Daher etablierte sie zusammen mit ihren Kollegen an der Poliklinik und dem Funktionsbereich für Rheumatologie an der Uniklinik in Düsseldorf seit 2011 einmal wöchentlich eine so genannte „run in“- Sprechstunde, bei der Patienten im Einzugsgebiet Düsseldorf mit Verdacht auf eine rheumatische Gelenk- oder Rückenerkrankung sowie entsprechender Überweisung vom Hausarzt sofort vorstellig werden können – ohne Terminvereinbarung und somit ohne Wartezeit. Von allen Vorstellungen im Zeitraum von fünf Jahren (n=1.592) wurde bei 388 Patienten eine „entzündlich-rheumatische“ Diagnose gestellt (z.B. RA (30%), SpA (25%), PMR (9%) und undiff. Arthritis (9%)).
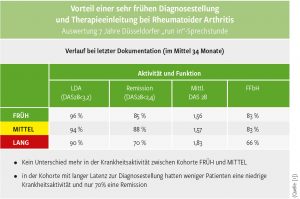
Abb. 1: Auswertung 7 Jahre Düsseldorfer “run in” Sprechstunde – Verlauf bei letzter Dokumentation.
Auswertungen einer „run in“- Ambulanz
In einer Auswertung über sieben Jahre „run in“- Sprechstunde wurden 140 Patienten mit RA standardisiert dokumentiert und leitliniengerecht behandelt und je nach Krankheitsdauer in drei Gruppen unterteilt („Früh“, „Mittel“ und „Lang“). Hierbei zeigte sich, dass bei RA eine sehr frühe Diagnosestellung verschiedene Vorteile bieten kann: So erreichten nach drei Monaten mehr Patienten der „Früh“-Kohorte eine niedrige Krankheitsaktivität beziehungsweise Remission (72%) als im Vergleich zu „Mittel“ und „Lang“ (56% und 50%). Im Behandlungsverlauf wurde bei der letzten Dokumentation nach durchschnittlich 34 Monaten festgestellt, dass die Krankheitsaktivität zwischen Kohorte „Früh“ und „Mittel“ in etwa gleich war. In der Kohorte mit langer Latenz zur Diagnosestellung hatten weniger Patienten eine niedrige Krankheitsaktivität und nur 70% eine Remission im Vergleich zu 85% bei „Früh“ und 88 Prozent bei „Mittel“ (s. Abb. 1). Außerdem war in der „Früh“-Kohorte seltener eine Eskalation der Basistherapie nötig als in der „Mittel“-Kohorte (MTX 63% vs. 71%; andere cDMARDs 27% vs. 36%; Biologika 13% vs. 25%). Eine Beendigung der Basistherapie war bei 17% in der Kohorte „Früh“ möglich, bei 9% in der Kohorte „Mittel“ und bei niemandem in Kohorte „Lang“. [1]
Fazit der „run in“-Sprechstunde
Daher lautet das Fazit von PD Dr. med. Fische-Betz, dass bei RA- Patienten, die sehr früh vorstellig werden, eine rasche Remission möglich ist, wofür seltener eine Therapieeskalation benötigt wird, so dass die Gesundheit und Funktion der betroffenen Gelenke unter Umständen erhalten bleibt. Patienten, die über ein Jahr bis zur Erstvorstellung benötigen, erreichen im Behandlungsverlauf kaum eine Verbesserung ihrer Gesundheit.
RA-assoziierte ILD
Zur RA-assoziierten interstitiellen Lungenerkrankung (ILD) gab Prof. Peter Härle, Chefarzt der Klinik für Rheumatologie, Klinische Immunologie und Physikalische Therapie in Mainz, zu bedenken, dass bei allen Basismedikamenten eine pulmonale Toxizität auftreten kann, jedoch die Kausalität zwischen Basismedikation und Lungentoxizität oft schwer nachzuweisen ist. Bei Verdacht auf RA-ILD rät der Experte, bei der Diagnose verschiedene Aspekte abzuklären, wie beispielsweise Komorbidität (Overlab mit Kollagenosen) sowie eine infektions- oder medikamentenbedingte (allergisch, toxisch oder autoimmun) Lungenbeteiligung.
Quelle: DGRh-Symposium “Was? Wie? Bei wem? – Interaktive Falldiskussion zu inflammatorischen Autoimmunerkrankungen“, 05. September 2019, Dresden; Veranstalter: Bristol-Myers Suibb
